新药速递 | 2023年3月获批的新药一览
看点:
- 多种罕见病迎来创新疗法
- FDA批准重磅偏头痛新药
- 日本批准全球首个治疗角膜内皮疾病的同种异体细胞疗法
- 国产肺癌1类新药「谷美替尼」获批上市
2023年3月,多款罕见病创新疗法获美国FDA批准上市,包括首款针对APDS的新药Joenja,首款针对Rett综合征的新药Daybue,以及针对罕见肿瘤MCC的PD-1单抗。此外,日本和中国也批准了多款创新药物,更多详情见下文。
01
美国FDA批准的新药
美国FDA药品审评和研究中心(CDER)在2023年3月批准了9款新药上市,包括3个新分子实体,4个新配方或新生产者,1个新药物组合,以及1个单抗。
表1. 2023年3月美国FDA批准的新药
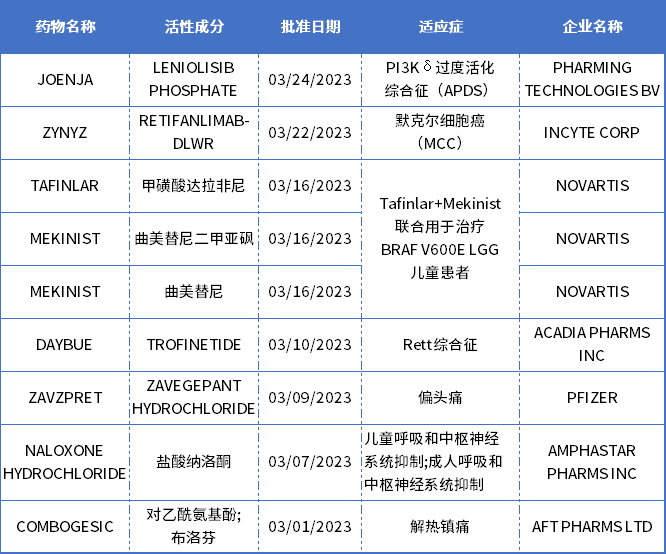
数据来源:美国FDA官网
本月FDA批准的3个新分子实体分别为JOENJA、DAYBUE和ZAVZPRET;1个BLA申请为Incyte公司的PD-1单抗ZYNYZ。
JOENJA
Joenja(leniolisib)是Pharming公司开发的一款选择性靶向磷脂酰肌醇3-激酶δ(PI3Kδ)的口服抑制剂,被FDA批准用于治疗12岁及以上患有磷脂酰肌醇3-激酶δ综合征(APDS)的成人/青少年患者。
APDS是由PIK3CD或PIK3R1基因突变引起的罕见的原发性免疫缺陷。Joenja最初由诺华公司开发,Pharming在2019年获得它的开发权益。Pharming公司新闻稿指出,这是FDA批准的首款针对APDS的药物。
DAYBUE
Daybue(trofinetide)是Acadia Pharmaceuticals公司开发的一种新型的IGF-1氨基末端三肽的类似物,获批用于治疗Rett综合征成人和2岁以上儿童患者。
Rett综合征是一种复杂的、累及多个系统的神经发育障碍,由大脑神经元和突触功能所必需的X连锁MECP2基因突变引起。Trofinetide通过减少神经炎症和支持突触功能来治疗Rett综合征的核心症状,此前曾获得美国FDA授予的优先审评资格、快速通道资格、孤儿药资格和罕见儿科疾病认定。Acadia新闻稿指出,这是FDA批准的首款治疗Rett综合征的药物。
ZAVZPRET
Zavzpret(zavegepant)是辉瑞公司开发的一款第三代高亲和力、高选择性的小分子降钙素基因相关肽(CGRP)受体拮抗剂,获批用于治疗成人患者急性偏头痛。
偏头痛是一种以持续4-72小时严重头痛发作为特征的神经疾病,伴随的其它症状包括恶心和对声光敏感。Zavegepant是首款获批上市的CGRP受体拮抗剂鼻内喷剂,可在15分钟内快速起效,缓解疼痛症状。
ZYNYZ
Zynyz(retifanlimab)是Incyte公司开发的一款人源化抗PD-1单克隆抗体,用于治疗移性或复发性局部晚期默克尔细胞癌(MCC)。
MCC是一种少见的原发性皮肤神经内分泌癌,retifanlimab为这一罕见癌种患者提供了新的治疗选择。Incyte公司表示还在继续研究Zynyz在其他肿瘤类型中的潜力,包括非小细胞肺癌、肛管鳞状细胞癌等。另外,2019年7月再鼎医药与Incyte公司达成研发协议,获得Retifanlimab在大中华区在血液和实体肿瘤领域的独家开发权益。
02
日本PMDA批准的新药
日本的处方药分类跟美国不太一样,该国药监局按照适应症分类,显示出PMDA以临床、医学及患者需求为导向,以解决某种疾病问题为出发点研发药物。
2023年3月,日本PMDA在批准了9款含有新活性成分药物,以及一款细胞疗法,详情见下表。
表2. 2023年3月日本PMDA批准的新药
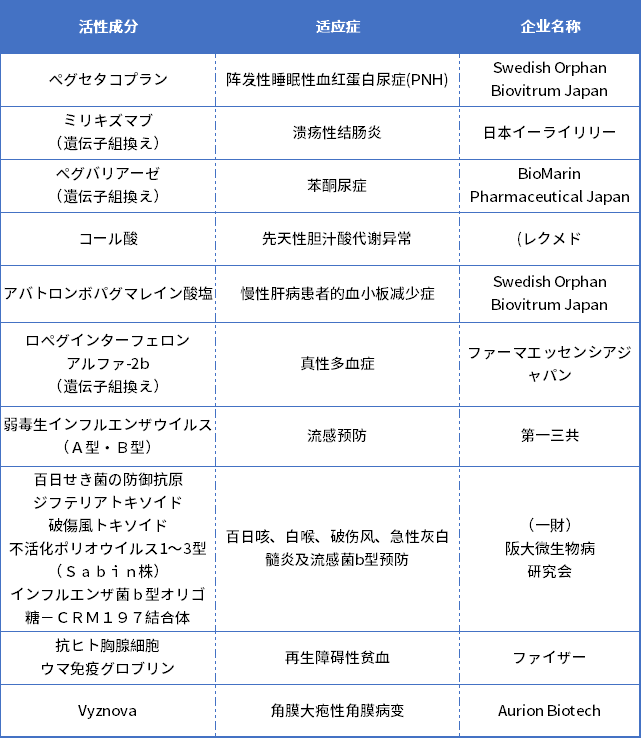
数据来源:PMDA官网
Vyznova
Vyznova是Aurion Biotech公司开发的一种新型细胞疗法,在日本获批用于治疗角膜大疱性角膜病变(bullous keratopathy of the cornea)。据Aurion公司新闻稿,这是全球首个获批用以治疗角膜内皮疾病的同种异体细胞疗法。
Vyznova是一项现货型、同种异体细胞疗法,来自捐赠者角膜的健康细胞通过Aurion专有的创新、多步骤培养,以产生完全分化的角膜内皮细胞。Aurion公司表示,每位捐赠者完全分化的角膜内皮细胞最终可用于治疗超过100只患者眼睛。
03
NMPA批准的新药
2023年3月,中国国家药品监督管理局(NMPA)仅批准了1款1类新药,来自上海海和药物。此外,NMPA还批准了1款2.2类新药,来自恒瑞医药。
表3. 2023年3月NMPA批准的国产新药

数据来源:NMPA官网、药智数据
谷美替尼片
谷美替尼(Glumetinib,代号:SCC244)是海和药物与中国科学院上海药物研究所合作研发的一款选择性c-Met激酶抑制剂,本次被NMPA附条件批准上市,用于具有间质-上皮转化因子(MET)外显子14跳变的局部晚期或转移性非小细胞肺癌的治疗。此前,谷美替尼曾被NMPA纳入突破性治疗品种名单,还被美国FDA授予具有MET基因变异的非小细胞肺癌孤儿药资格。
盐酸右美托咪定鼻喷剂
盐酸右美托咪定是一款α2-肾上腺素能受体激动剂,此前市场上有盐酸右美托咪定氯化钠注射液和盐酸右美托咪定注射液两种剂型,生产企业包括扬子江药业、恒瑞医药、恩华药业、四川国瑞药业等数十家药企。
「盐酸右美托米啶鼻喷雾剂」为恒瑞医药申报的化药2.2类新药,是该领域首款鼻喷制剂,此前该申请曾被药监局授予优先审评资格,本次获批用于儿童术前镇静。
除了国产新药,本月还有4款进口新药获得NMPA批准,详情见下表:
表4. 2023年3月NMPA批准的进口新药

数据来源:NMPA官网、药智数据
双羟萘酸曲普瑞林是一种天然促性腺激素释放激素(GnRH)的类似物,早在2008年11月,就国家药监局批准用于局部晚期或转移性前列腺癌的治疗。本次获批新适应症:局部晚期和转移性前列腺癌、子宫内膜异位症、中枢性性早熟(8岁前的女孩和10岁前的男孩)。值得一提的是,丽珠制药的2.2类新药注射用双羟萘酸曲普瑞林微球已在2021年3月获批临床。
阿可替尼(acalabrutinib,商品名:康可期)是阿斯利康开发的新一代选择性BTK抑制剂,曾获得美国FDA授予优先审评资格、突破性疗法认定和孤儿药资格。2017年,阿可替尼首次获美国FDA批准,用于二线治疗套细胞淋巴瘤(MCL),此后又获了慢性淋巴性白血病(CLL)、小细胞淋巴瘤(SLL)适应症。本次在中国获批适应症为二线治疗MCL。
甲氨蝶呤注射液(预充式)是medac公司开发的皮下给药小容量甲氨蝶呤产品,专门设计用于治疗类风湿关节炎等自身免疫性疾病。康哲药业拥有该药在中国大陆、香港地区、台湾地区的开发和商业化独家权益,本次在国内获批适应症为:治疗对常规疗法不敏感的严重、顽固、致残性银屑病。
依拉环素(Xerava)是一种潜在同类最佳新型合成非胃肠道的四环素类药物,目前已在美国、欧盟、英国和新加坡被批准用于治疗复杂性腹腔内感染。云顶新耀拥有该药在大中华区域(包括台湾、香港、澳门)、韩国和新加坡开发和商业化的独家权益。本次在国内获批用于治疗成人复杂性腹腔内感染。
4月,又将有哪些新药获得批准?欢迎关注博药微信公众号,小编将为您持续跟踪报道。

责任编辑:琉璃
声明:本文系本网站转载内容,图片、文字版权归原作者所有,转载目的在于传递更多信息,并不代表本平台观点。如涉及作品内容、版权和其它问题,请在本平台留言,我们将在第一时间处理。



 江西仁和中方医药股份有限公司
All Rights Reserved
江西仁和中方医药股份有限公司
All Rights Reserved